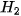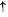(Trang 47)
Học xong bài học này, em có thể:
• Nêu được khái niệm acid (tạo ra ion H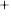 ).
).
• Tiến hành được thí nghiệm của hydrochloric acid (làm đổi màu chất chỉ thị; phản ứng với kim loại), nêu và giải thích được hiện tượng xảy ra trong thí nghiệm (viết phương trình hoá học) và rút ra nhận xét về tính chất của acid.
• Trình bày được một số ứng dụng của một số acid thông dụng (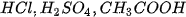 ).
).
![]() Các loại quả trong hình dưới đây có đặc điểm gì giống nhau? Theo em, vì sao chúng lại có đặc điểm giống nhau đó?
Các loại quả trong hình dưới đây có đặc điểm gì giống nhau? Theo em, vì sao chúng lại có đặc điểm giống nhau đó?
|
a) Quả sấu |
b) Quả me |
c) Quả chanh |
Hình 8.1. Một số loại quả thường gặp
I. KHÁI NIỆM ACID
| Giấm ăn hoặc chanh thường được cho vào nước chấm để tạo ra vị chua, sấu, me hoặc cà chua cũng tạo ra vị chua cho một số món ăn. Vị chua của giấm ăn và các loại quả ở trên được tạo ra bởi một loại hợp chất gọi là acid. Khi tan trong nước, acid tạo ra ion H Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H Acid → ion H Ví dụ: HCl → H Hydrochloric acid Ion hydrogen Ion chloride
Sulfuric acid Ion hydrogen Ion sulfate |
|
(Trang 48)
II. TÍNH CHẤT HOÁ HỌC CỦA ACID
1. Làm đổi màu chất chỉ thị
Tiến hành thí nghiệm sau để tìm hiểu về sự làm đổi màu chất chỉ thị của dung dịch acid.
|
a) Nước làm quỳ tím đổi màu. b) Dung dịch acid làm quỳ tím đổi màu. Đề xuất một thí nghiệm để xác định ý kiến đúng trong hai ý kiến trên. 3. Lần lượt nhỏ lên ba mẩu giấy quỳ tím mỗi dung dịch sau: a) Nước đường. b) Nước chanh. c) Nước muối (dung dịch NaCl). Trường hợp nào quỳ tím sẽ chuyển sang màu đỏ? |
Chuẩn bị • Dụng cụ: Mặt kính đồng hồ, ống hút nhỏ giọt. • Hoá chất: Dung dịch HCl loãng, giấy quỳ tím. Tiến hành • Đặt mẩu giấy quỳ tím lên mặt kính đồng hồ, lấy dung dịch HCl loãng và nhỏ một giọt lên mẫu giấy quỳ tím. • Mô tả các hiện tượng xảy ra. Các dung dịch sulfuric acid loãng, acetic acid,... cũng làm giấy quỳ tím chuyển màu tương tự như với dung dịch hydrochloric acid. Dung dịch acid làm quỳ tím chuyển sang màu đỏ. Quỳ tím được dùng làm chất chỉ thị màu để nhận ra dung dịch acid. |
2. Tác dụng với kim loại
Tiến hành thí nghiệm sau để tìm hiểu về phản ứng của acid với kim loại.
![]() Thí nghiệm 2
Thí nghiệm 2
Chuẩn bị
• Dụng cụ: Giá để ống nghiệm, ống nghiệm, ống hút nhỏ giọt.
• Hoá chất: Dung dịch HCl loãng, Zn viên.
Tiến hành
• Cho một viên Zn vào ống nghiệm, sau đó cho thêm vào ống nghiệm khoảng 2 mL dung dịch HCI loãng.
• Mô tả các hiện tượng xảy ra.
• Những dấu hiệu nào chứng tỏ có phản ứng hoá học giữa dung dịch HCl và Zn?
(Trang 49)
| Dung dịch HCl đã phản ứng với Zn tạo ra chất khí. Phương trình hóa học của phản ứng trên như sau: Zn + 2HCl → Zinc Hydrochloric acid Zinc chloride Hydrogen Dung dịch các acid khác như sulfuric acid loãng, acetic acid,... cũng có phản ứng hoá học với nhiều kim loại tạo ra muối và khi hydrogen. Dung dịch acid tác dụng được với nhiều kim loại tạo ra muối và khí hydrogen Acid + Kim loại → Muối + Hydrogen.
a) Dung dịch b) Dung dịch HCl loãng tác dụng với Mg. III. ỨNG DỤNG CỦA MỘT SỐ ACID1. Hydrochloric acid (HCI)Hydrochloric acid có trong dạ dày của người và động vật giúp tiêu hoá thức ăn. Hydrochloric acid được sử dụng nhiều trong công nghiệp. Một số ứng dụng quan trọng của hydrochloric acid được trình bảy trong hình 8.2.
Hình 8.2. Một số ứng dụng của hydrochloric acid |
|
------------------------------------------------
(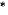 ) Riêng
) Riêng 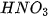 ,
, 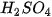 đặc tác dụng với kim loại sẽ được học sau.
đặc tác dụng với kim loại sẽ được học sau.
(Trang 50)
2. Sulfuric acid (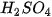 )
)
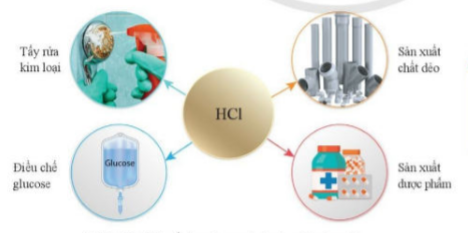
Sulfuric acid là một hoá chất quan trọng được sử dụng nhiều trong công nghiệp. Một số ứng dụng quan trọng của sulfuric acid được trình bày trong hình 8.3.
|
Hình 8.3. Một số ứng dụng của Sulfuric acid
|
3. Acetic acid (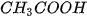 )
)
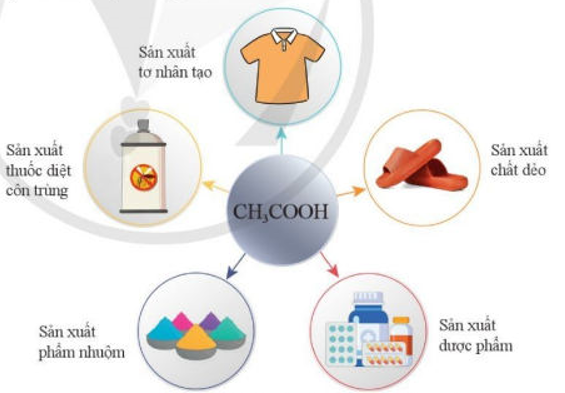
Acetic acid là một acid hữu cơ có trong giấm ăn với nồng độ khoảng 4%. Một số ứng dụng của acetic acid được trình bày trong hình 8.4.
|
|
Hình 8.4. Một số ứng dụng của acetic acid
|
![]() • Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H
• Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H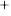 .
.
• Dung dịch acid có vị chua, làm quỳ tím chuyển sang màu đỏ, tác dụng với nhiều kim loại tạo ra khí hydrogen.
• Hydrochloric acid, sulfuric acid và acetic acid là những acid có nhiều ứng dụng trong đời sống và trong công nghiệp.





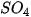
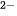
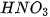 ).
).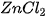 +
+